고지방식이를 섭취한 마우스에서 흰점박이꽃무지 유충의 효소 가수분해물이 당대사 및 지질대사에 미치는 영향
This is an Open-Access article distributed under the terms of the Creative Commons Attribution Non-Commercial License (http://creativecommons.org/licenses/by-nc/3.0) which permits unrestricted non-commercial use, distribution, and reproduction in any medium, provided the original work is properly cited.
Abstract
There have been few studies to date on physiologically active peptides derived from Protaetia brevitarsis larvae (PBL). This study aimed to examine the effects of PBL enzyme hydrolysates on glucose and lipid metabolism in mice fed a high-fat diet. Four-week-old male C57BL/6J mice were acclimated for one week. They were then divided into three groups: the normal fat diet-fed group (ND; n = 5), the high-fat diet-fed group (HD; n = 6), and the high-fat diet-fed group that was orally administered PBL enzyme hydrolysate (200 mg/kg/day, 7 times/week) (HDP; n = 6). After 7 weeks on the experimental diet, dietary intake decreased significantly in the HD group compared with the ND group, but it was not significant in the HDP group. Low-density lipoprotein cholesterol (LDL-C) and triglyceride (TG) were significantly increased in the HD group compared with the ND group but were not reduced in the HDP group. In the oral glucose tolerance test (OGTT) glucose levels at 30 minutes were significantly higher in the HD group than in the ND group and tended to decrease in the HDP group. Tumor necrosis factor-alpha (TNF-α) mRNA expression was significantly increased in the HD group compared with the ND group, but tended to decrease in the HDP group compared with the HD group. In conclusion, in mice fed a high-fat diet, PBL enzyme hydrolysate inhibited the rise in blood glucose during the initial 30 minutes of OGTT and showed a tendency to lower expression of TNF-α genes in the liver tissue. Further studies are needed to clarify the concentration-specific and long-term effects of PBL enzyme hydrolysate on metabolic improvement in mice fed a high-fat diet.
Keywords:
obesity, Protaetia brevitarsis larvae, high-fat diet, glucose tolerance, tumor necrosis factor-αⅠ. 서론
비만은 에너지 섭취와 소비 간의 불균형으로 인해 체지방이 비정상적이거나 과도하게 축적 및 분포되는 상태로, 지난 수십 년간 전 세계적으로 유병률이 급격히 증가하면서 중요한 공중보건 문제로 대두되고 있다. 우리나라 20세 이상 성인의 비만 유병률은 2012년 30.2%(남성 37.3%, 여성 23.4%)에서 2021년 38.4%(남성 49.2%, 여성 27.8%)까지 1.27배 증가하였다(Jeong et al. 2024). 같은 기간 동안 아동ㆍ청소년(6-18세)의 비만 또한 9.7%에서 19.3%까지 약 2배 증가하여 우리나라에서도 비만 유병률이 지속적으로 증가함을 보여준다. 저소득 및 중간소득 국가에서는 여전히 겪고 있는 감염성 질환과 영양결핍 문제와 동시에 과체중과 비만의 유병률이 증가하여 이중 영양 부담(double burden of malnutrition)에 직면해 있기도 한다(Winichagoon & Margetts 2017).
비만은 인슐린 저항성, 대사증후군, 이상지질혈증, 고혈압, 제2형 당뇨병, 비알코올성 지방간 질환(non-alcoholic fatty liver disease, NAFLD), 심혈관계 질환, 우울증, 인지 기능 저하 및 암 등 다양한 동반 질환의 발생 위험을 유의적으로 증가시킨다(Petrie et al. 2018; Tyrrell et al. 2019; Larsson & Burgess 2021; Francque & Dirinck 2023). 또한, 의료비 증가에도 상당한 영향을 미치는데, 과체중 및 비만으로 인한 전 세계적 경제적 비용은 2020년 기준 약 2조 달러 미만에서 2030년에는 3조 달러를 초과하고, 2060년에는 무려 18조 달러 이상에 이를 것으로 예측된바 있다(Okunogbe et al. 2022). 따라서 비만으로 인한 예방 가능한 사망과 사회경제적 비용을 감소시키기 위해서는 비만을 예방하고 치료할 수 있는 천연물 유래의 안전한 기능성 소재 개발이 필요하다.
최근, 식용 곤충은 식량 자원의 지속가능성과 기능성 식품 개발 측면에서 새로운 대안으로 주목받고 있다. 곤충은 단백질, 불포화지방산, 비타민, 미네랄 등을 풍부하게 함유하고 있을 뿐만 아니라, 환경친화적이고 생산 효율이 높은 장점을 지닌다(Park & Yun 2018). 2025년 기준 우리나라에서 식용이 가능한 곤충은 총 10종으로 일반 식품원료가 9종이고 한시적 식품원료가 1종이다. 그중 흰점박이꽃무지 유충(Protaetia brevitarsis larvae; PBL)은 2016년에 식품공전에 원료로 등록되어 현재 곤충산업 1차 산물 판매액 중 1위를 차지하고 있으며(Ministry of Agriculture, Food and Rural Affairs 2025), 기능성에 대한 과학적 근거가 점차 확대되고 있다. Park et al.(2024)은 PBL의 70% 에탄올 추출물이 Hep3B 세포에서 LPS 유발 염증과 철분 의존성 세포사멸에 대해 억제 효과를, Jang et al.(2023)은 PBL이 마우스 골수 유래 대식세포에서 RANKL 유도 파골세포 형성에 대한 억제 효과를 나타냈다고 보고하였다 또한, PBL의 항비만 효과(Ahn et al. 2019), 항당뇨 효과(Park et al. 2021), 항산화 및 항염증 효과를 통한 에탄올 유도 간 손상 보호 효과(Hwang et al. 2020) 등도 밝혀져 있다.
한편, 단백질을 효소 가수분해할 경우 식품 단백질에서 유래된 펩타이드는 아미노산 조성, 서열, 소수성 및 길이에 따라 영양학적 특성 외에도 항고혈압, 항산화, 항혈전, 혈당 강하, 콜레스테롤 저하 및 항균 작용 등 다양한 생리활성을 나타낼 수 있다(Nasri 2017). 따라서, 본 연구에서는 고지방식이를 섭취한 마우스에서 PBL 효소 가수분해물이 체중 변화, 혈당, 내당능 및 혈중 지질 지표에 미치는 영향을 분석함으로써, PBL 효소 가수분해물의 당대사 및 지질대사 개선 효과를 규명하고자 하였다. 본 연구 결과는 PBL 효소 가수분해물의 비만 관련 대사성 질환을 예방하고 개선시키기 위한 소재로서의 활용 가능성에 대한 기초자료를 제시할 것이다.
Ⅱ. 연구방법
1. PBL 효소 가수분해물 제조
흰점박이꽃무지 분말 20 g을 800 mL의 증류수에 현탁한 후 121℃에서 15분간 고압멸균을 실시하였다. 이후 시료를 냉각시키고 단백질 가수분해효소인 trypsin(Sigma-Aldrich, St, Louis, MO; T4799) 0.2 g을 첨가하여 150 rpm 조건에서 6시간 동안 진탕배양기(Dasol Scientific, Hwaseong, Korea; DS-310F)를 이용하여 효소 가수분해를 수행하였다. 80℃에서 10분간 효소의 실활 과정을 거친 후 2,000 rpm으로 원심분리하여 상징액을 분리하였다. 분리된 상징액은 진공감압 여과기를 통해 여과한 후 동결건조 과정을 거쳐 최종 시료를 제조하였다. 본 연구에 사용된 PBL 효소 가수분해물은 경상남도농업기술원 유용곤충연구소로부터 제공받아 -80℃에서 보관하며 사용하였다.
2. 실험동물 및 식이
실험동물은 생후 4주령의 수컷 C57BL/6J 마우스를 중앙실험동물(Seoul, Korea)에서 구입하여 사용하였다. 각 동물은 통제된 환경(실온 22 ± 2°C, 상대습도 55 ± 5%, 암주기 12시간/12시간)에서 개별 사육하였다. 1주일간의 적응 후에, 마우스를 무작위로 정상지방식이 섭취군 (normal-fat diet, ND; n = 5), 고지방식이 섭취군 (high-fat diet, HD; n = 6), 고지방식이 및 PBL 효소 가수분해물 섭취군 (high-fat diet treated with PBL, HDP; n = 6)군으로 분류하였다. 실험식이의 구성은 Table 1에 제시되어 있다. ND군의 정상지방식이는 지방에서 비롯된 열량이 총 열량의 10%(Saeronbio Inc, Uiwang, Korea; D12450B)를 차지하였고, HD와 HDP군의 고지방식이는 지방으로부터 열량이 60%(Saeronbio Inc; D12492)를 차지하였다. HDP군에는 PBL 효소 가수분해물을 200 mg/kg b.w./day 수준으로 7주간 경구 투여하였으며, ND군과 HD군에는 동일한 양의 식염수를 경구 투여하였다. PBL 효소 가수분해물의 투여 수준은 160 mg/kg 수준에서 비만 마우스에 대해 항비만 및 간 보호 효과가 나타났다는 이전 연구를 근거로 선택되었다(Lee et al. 2022). 실험 기간 내내 식이와 물은 자유롭게 섭취할 수 있도록 하였고, 체중은 주 1회, 식이 섭취량은 주 2회 일정한 시간에 측정하였다. 모든 실험 설계 및 절차는 경상대학교 동물실험윤리위원회 (GNU-230419-M0069-01)의 승인을 받아 시행하였다.
3. 경구 당부하 검사(Oral glucose tolerance test, OGTT)
경구 당부하 검사는 실험 종료 1주일 전에 수행하였다. 마우스를 12시간 절식시킨 다음 꼬리정맥에서 채혈하여 초기 혈당을 측정하고 75% 포도당 용액을 2 g/kg b.w.의 수준으로 경구투여 한 후 30, 60, 120분에 해당하는 혈당 농도를 측정하였으며, 이를 통해 내당능(Glucose tolerance) 변화를 확인하였다. 혈당은 꼬리로부터 채혈하여 혈당측정기(Roche Diagnostic, Mannheim, Germany; ACCU-CHEK Instant S)를 통해 측정하였다.
4. 혈액 및 조직 채취
실험 종료 후에 12시간 절식시킨 마우스를 CO2로 마취한 뒤 복부 대동맥에서 혈액을 채취하였다. 채취한 혈액은 원심분리기(GYROZEN Co., Gyeonggi, Korea)를 이용하여 4°C에서 3,000 rpm으로 20분간 원심분리하여 혈청을 분리하였다. 복부 절개 후 적출한 간 조직 일부는 RNAprotect Reagent (Qiagen, Valencia, CA)에 즉시 담근 후 사용 시까지 -80°C에서 보관하였다. 나머지 간 조직과 지방 조직은 식염수로 세척하고 무게를 측정하였다. 측정 후 잔여 조직은 액체 질소에 급속 냉동한 후 -80°C에서 보관하였다.
5. 혈액 생화학적 분석
혈청의 triglyceride (TG), total cholesterol (TC), high-density lipoprotein-cholesterol (HDL-C), low-density lipoprotein-cholesterol (LDL-C), 공복 혈당은 시판 분석 키트(Asan Pharm. CO., Seoul, Korea)를 사용하여 측정하였다. 인슐린 또한 상용 키트(Crystal Chem, Illinois, Chicago)로 분석하였다. 인슐린 저항성 지수(homeostasis model assessment of insulin resistance, HOMA-IR)는 아래의 식에 의해 계산하였다(Jang et al. 2012).
HOMA-IR = Fasting glucose (mg/dL) × Fasting insulin (mU/L)/405
6. Real-time RT-PCR 분석
간 조직으로부터의 총 RNA는 RNeasy Protect Mini Kit(Qiagen, Hilden, Germany)를 사용하여 추출하였다. RNA 농도 및 순도는 NanoDrop Lite Plus Spectrophotometers(Thermo Scientific™, MA; NDLPLUSPRGL)을 사용하여 측정하였다. 분리된 RNA는 QuantiTect Reverse Transcription Kit(Thermofisher, Vilnius, Lithuania)를 이용하여 cDNA로 역전사하였다. Real-time RT-PCR 분석은 합성된 cDNA를 이용하여 SYBR Green Supermix (Bio-Rad, Hercules, CA)와 CFX Opus 96 Real-time PCR System (Bio-Rad)을 사용하여 수행하였다. PCR 반응 조건은 95℃에서 3분간 초기 변성 단계를 거친 후, 95℃에서 15초, 60℃에서 30초, 72℃에서 30초를 1 cycle로 하여 총 40 cycles로 진행하였다. 사용된 primer 서열은 다음과 같다; β-actin: 5'-CCAGCCTTCCTTCTTGGGTAT-3'(Forward), 5'-TTGGCATAGAGGTCTTTACGG'(Reverse); TNF-α: 5'-TGTCTCAGCCTCTTCTCATT-3'(Forward), 5'-AGATGATCTGAGTGTGAGGG-3'(Reverse). Threshold cycle(Ct) 값은 제조사의 지침에 따라 형광 신호의 변화를 분석하여 상대 정량 값을 산출하였다. 각 유전자의 발현 수준은 동일 시료에서 측정한 β-actin 발현량으로 보정하였고, HD군과 HDP군의 ΔCt 값은 ND 군의 평균 ΔCt 값으로 정규화하였다.
7. 통계처리
모든 실험결과에 대한 통계분석은 IBM SPSS® Statistics for windows 프로그램을 이용하여 수행하였다. 세 개의 실험군 간의 유의성 검정을 위해 일원분산분석(one way analysis of variance, ANOVA)을 실시한 후, Duncan의 다중범위검정(Duncan’s multiple range test)을 이용하여 사후 분석을 수행하였다. 모든 실험 결과는 평균 ± 표준편차로 나타내었으며 P < 0.05 수준에서 통계적 유의성을 검증하였다.
Ⅲ. 결과
1. 체중, 식이섭취량 및 조직무게 변화
7주 동안의 실험식이 공급 후 체중 증가량은 군간에 유의한 차이는 보이지 않았으나, 고지방식이 섭취군인 HD군(3.40 ± 1.30 g/day)과 HDP군(3.27 ± 1.57 g/day)에서 ND군(2.00 ± 1.42 g/day)에 비해 증가한 경향을 보였다. 일일 식이 섭취량은 고지방 식이를 섭취한 HD군(2.14 ± 0.14 g/day)과 HDP군(2.08 ± 0.08 g/day)에서 ND군(2.56 ± 0.21 g/day) 대비 유의하게 낮게 나타났다(P<0.05). 한편, 식이 효율(Food efficiency ratio)이나 에너지 효율(Energy efficiency ratio)은 ND군에 비해 HD군과 HDP군에서 높은 경향을 보였으나, 통계적 유의성은 관찰되지 않았다(Table 2). 실험동물의 간 조직 무게는 ND군(0.82 ± 0.13 g)에 비해 HD군(0.75 ± 0.03 g)과 HDP군(0.77 ± 0.09 g)에서 증가하지 않았으나 신장 주변 지방, 복부 지방 조직의 무게는 ND군(0.46 ± 0.12 g, 0.07 ± 0.04 g)에 비해 HD군(0.59 ± 0.15 g, 0.10 ± 0.04 g)에서 약 1.3배, 1.4배 증가하였고(P>0.05) PBL 효소 가수분해물이 간 조직이나 지방 조직 무게에 유의한 영향을 미치지 못하였다(Table 3).
2. 혈중 중성지질 및 콜레스테롤
혈중 중성지질 및 콜레스테롤 농도를 Table 4에 제시하였다. TG의 경우, ND군(168.17 ± 4.54 mg/dL)에 비해 HD군(194.83 ± 17.16 mg/dL)에서 유의하게 증가하였으나, 고지방식이 섭취군에서 PBL 효소 가수분해물의 투여는 중성지질에 유의한 영향을 미치지 못하였다(HDP군: 203.89 ± 27.11 mg/dL). LDL-C 또한, ND군(296.33 ± 13.20 mg/dL) 대비 HD군(318.00 ± 4.54 mg/dL)에서 유의하게 증가하였고, HDP군(312.78 ± 31.39 mg/dL)에서는 HD군 대비 유의한 변화를 나타내지 못하였다. 반면, TC와 HDL-C 수치는 군 간에 유의한 차이를 나타내지 않았다(Table 4).
3. 혈중 당, 인슐린 및 HOMA-IR
공복 혈당, 인슐린, 및 HOMA-IR 분석 결과를 Table 5에 제시하였다. 공복 혈당은 ND 군에서 높게 나타났으나 통계적으로 유의한 차이는 나타나지 않았다. 공복 인슐린 농도 또한 세 군간에 유의한 차이를 보이지 않아, 인슐린저항성 지수인 HOMA-IR에도 고지방식이나 PBL 효소 가수분해물의 처리는 유의한 영향을 미치지 않았다(Table 5).
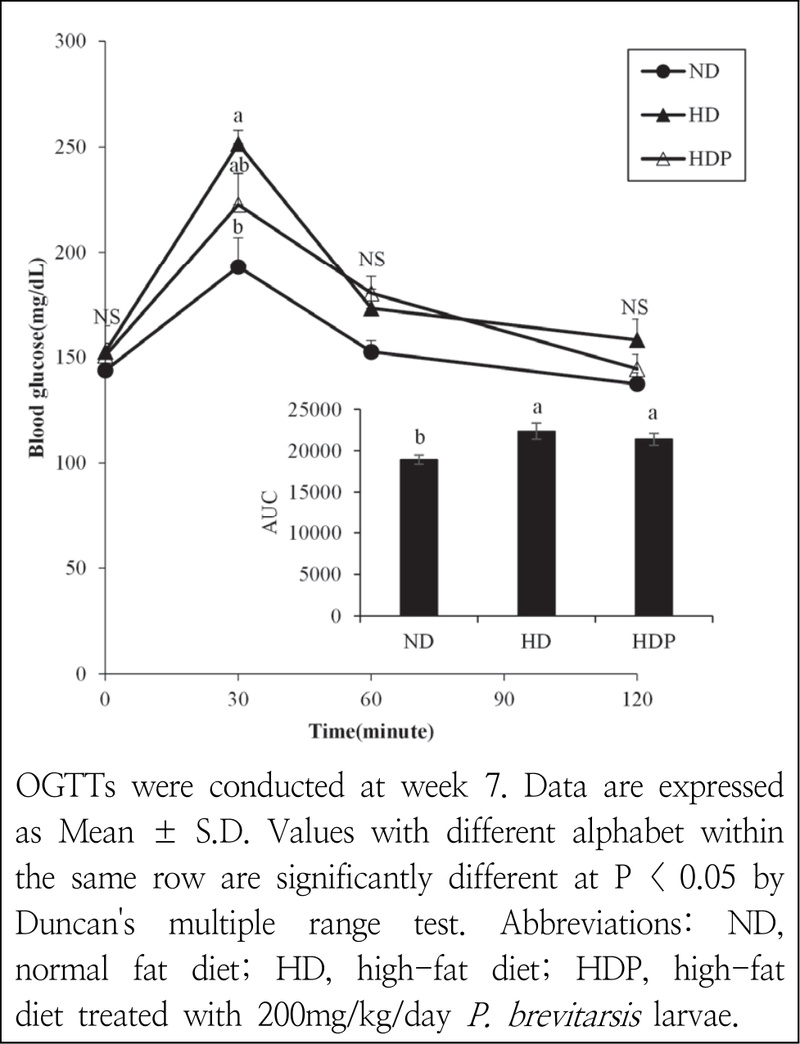
4. 내당능(OGTT)
공복 시 혈당부터 시작하여 당을 경구 투여한 후 30, 60, 120분의 혈당을 Fig. 1에 제시하였다. 공복 혈당은 군 간에 유의한 차이를 보이지 않았으나, 당 투여 후 30분에 ND군에 비해 HD군의 혈당이 유의하게 증가하였고, PBL 효소 가수분해물의 투여는 혈당을 ND군의 수준으로 회복시키지는 못하였으나, HD군에 비해 감소시키는 경향을 나타내었다. 30분 시점에서 모든 군의 혈당이 급격히 상승하였으며 이후 점차 감소하는 것으로 나타났고, 혈당 반응 곡선하면적(area under the curve; AUC) 분석 결과, HD군과 HDP군에서 ND군에 비해 유의하게 증가하였다(Fig. 1).
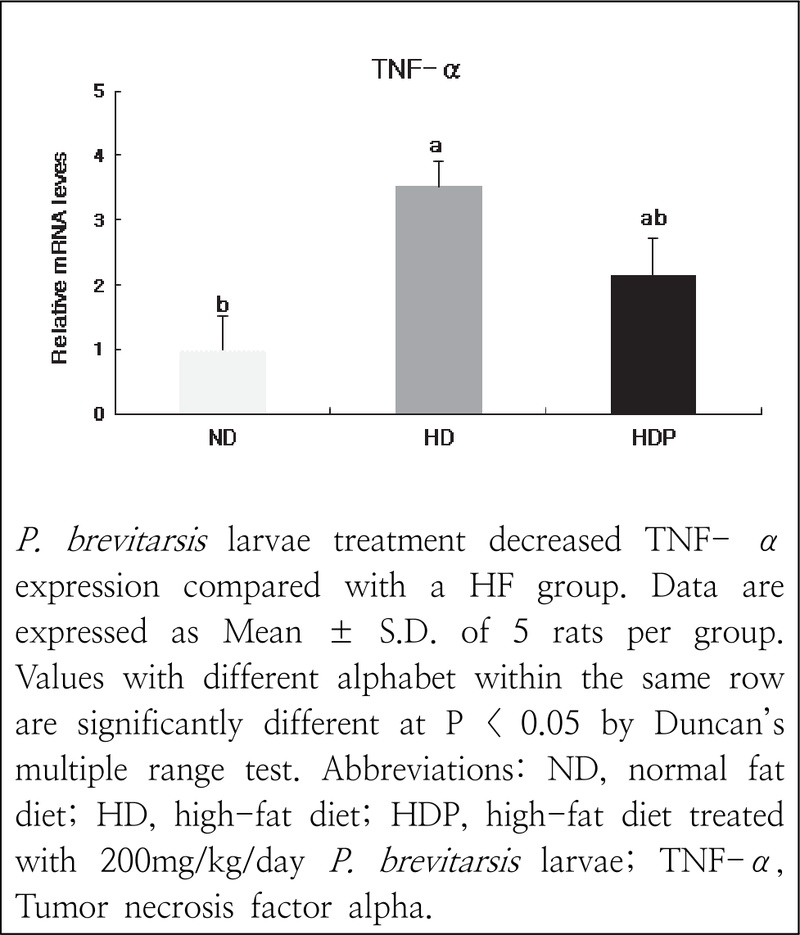
5. 간 조직 TNF-α mRNA 발현
간 조직에서 TNF-α 유전자의 mRNA 발현량을 분석한 결과는 Figure 2에 나타내었다. 염증성 사이토카인인 TNF-α의 경우 HD군(3.53 ± 0.38)에서 ND군(1.00 ± 0.51)에 비해 3배 이상 높은 발현을 보였으며(P<0.05), HDP군(2.15 ± 0.59)에서 HD군 대비 mRNA 발현 수준이 61% 수준으로 감소하는 경향을 보였다(Fig. 2).
Ⅳ. 고찰
본 연구는 고지방식이를 섭취한 마우스에서 PBL 효소 가수분해물을 7주간 경구투여 하였을 때 당 대사, 지질 대사 및 염증 반응에 미치는 영향을 알아보기 위해서 혈당 대사 지표(공복 혈당, 인슐린, HOMA-IR, 및 OGTT), 지질 대사 지표(TG, TC, LDL-C, HDL-C), 염증 조절 인자(TNF-α mRNA 발현)를 조사하였다.
본 연구 결과, HD군에서 ND군에 비해 식이섭취량은 유의하게 감소하고, TG와 LDL-C이 유의하게 증가하였으며, OGTT 결과에서 포도당 용액 섭취 후 30분의 혈당은 HD군에서 ND군에 비해 유의하게 증가하였다. 또한, HD군에서 ND군에 비해 간 조직의 염증(TNF-α) mRNA 발현 수준이 유의하게 증가하였다. 기존 연구 결과들에 따르면, 장기간 고지방식이 섭취는 intestinal barrier 손상, inflammatory signaling pathways 활성, 미토콘드리아 기능장애 유발, 병원성 항생제 내성 유발 등을 일으켜 국소 및 전신 염증을 활성화해, 결국은 지질 및 에너지 대사를 방해하여 인슐린 저항성 및 이상지질혈증이 유발될 수 있다고 보고된다(Tang et al. 2024).
반면, 체중 증가량과 간 및 지방 조직 무게, 공복 혈당 및 인슐린, 그리고 이 두 수치를 활용한 계산치인 HOMA-IR은 ND군과 HD군에서 유의한 차이를 나타내지 않았다. 이것은 첫째, 고지방식이 섭취군의 식이 섭취량 감소에 의한 섭취 에너지의 감소로 인한 것일 수 있다. 본 연구에서 사용한 정상지방식이의 에너지는 g 당 3.85 kcal, 고지방식이의 에너지는 g 당 5.24 kcal로 고지방식이의 에너지가 1.4배 높았으나, 정상지방식이 섭취군에 비해 고지방식이 섭취군에서 유의한 식이섭취량의 감소가 나타났다. 결국 실험기간 동안의 평균 일일 섭취 에너지는 ND군, HD군, HDP군에서 각각 9.8, 11.2, 10.9 kcal/day로 고지방식이군의 에너지 섭취가 정상지방식이군에 비해 1.1배 증가하였다. 둘째, 본 연구에서 사용한 정상지방식이(Saeronbio Inc, D12450B)가 지방 함량은 낮지만 정제당(sucrose) 비율이 높은 조성(35% w/w)으로 ND군의 비만 및 혈당 관련 지표에 영향을 준 것일 수 있다. Blaisdell et al.(2014)의 연구에서 6개월 동안 현재 연구의 정상지방식이와 동일한 식이(D12450B)를 섭취시켰을 때 일반 사료에 비해 유의미하게 체중이 증가하였다.
본 연구 결과, 고지방식이를 섭취한 마우스에서 TG, LDL-C이 정상지방식이 섭취 마우스에 비해 유의하게 증가하였지만, PBL 트립신 효소 가수분해물은 고지방식이로 인한 혈중 TG, LDL-C 증가를 유의적으로 낮추지는 못하였다. 기존의 연구를 살펴보았을 때, PBL 에탄올 추출물을 고지방식이로 유도한 비만 C57BL/6J mice에 7주간 투여한 결과, 체중 증가, 부고환 및 피하 지방 무게 감소, 간 무게 감소, 글루타티온 퍼옥시다제(GPx) 및 CAT 증가, 간에서 lipid droplet 축적 감소, 혈중 TG, TC 및 LDL-C 수치 감소 효과가 보고되었다(Ahn et al. 2019). 뿐만 아니라, 고지방식이를 섭취한 C57BL/6J mice에게 PBL 에탄올 추출물을 14주 동안 투여 한 결과, 장(intestinal) 및 고환 지방 조직, 체중 및 간 조직 무게가 감소하였고 혈중 TG와 TC가 감소하였으며, 혈중 adiponectin 농도가 증가하였다(Im et al. 2018). 이러한 본 연구 결과와 선행연구 간의 차이는 PBL의 추출 및 가수분해 방식 등에 따른 생리활성 성분의 차이에서 비롯되었을 가능성이 있을 것이다.
PBL 단백질 가수분해물은 우수한 항산화 효과를 보여주고 있다. Lee et al.(2017)은 다섯 가지의 프로테아제(alcalase, bromelain, flavourzyme, neutrase, papain)로 제조된 PBL 단백질 가수분해물의 항산화 활성을 조사하였다. 2,2-diphenyl-1-picrylhydrazyl (DPPH) RC50 값은 alcalase 151.99 μg/ mL, flavourzyme 149.28 μg/mL neutrase 131.43 μg/mL로써, neutrase PBL 단백질 가수분해물의 DPPH 라디칼 소거 활성이 가장 높았다. 2,2’-azino-bis(3-ethylbenzothiazoline-6-sulfonic acid) (ABTS) RC50값은 alcalase 34.59 μg/mL, neutrase 42.49 μg/mL, flavourzyme 44.34 μg/mL 순으로 alcalase PBL 단백질 가수분해물의 ABTS 라디칼 소거 활성이 가장 높았다. Hydrogen peroxide RC50값은 alcalase 46.31 μg/mL, neutrase 58.16 μg/mL, flavourzyme 59.30 μg/mL로 alcalase PBL 단백질 가수분해물의 hydrogen peroxide 라디칼 소거 활성이 가장 높았다. Park & Lee(2023)는 PBL 단백질 가수분해물의 생리활성을 조사 한 결과, PBL flavourzyme 단백질 가수분해물이 Nrf2 매개 유도를 통해 AML12 마우스 간세포에서 H2O2 유도 세포 독성을 감소시킴을 관찰하였다.
본 연구 결과, PBL 효소 가수분해물은 고지방식이로 인한 간 조직의 염증 관련 인자인 TNF-α의 발현을 낮추는 경향을 보였다. PBL과 PBL 효소 가수분해물의 항염증 효과를 보여주는 연구 결과는 본 연구에서 사용된 PBL의 트립신 가수분해물의 항염증 효과를 뒷받침해준다. Park et al.(2024)의 연구에서 PBL의 70% 에탄올 추출물은 Hep3B 세포에서 LPS로 유도된 세포 사멸을 효과적으로 억제하였으며, TNF-α, IL-1β, 및 IL-6와 같은 염증성 사이토카인의 생성과 NF-κB(nuclear factor-κB) 신호 전달 경로를 유의하게 억제하였다. Kwon et al.(2023)은 비만 유도의 대장염 마우스 모델에서 PBL을 단백질 가수분해효소(alcalase) 처리하여 160 mg/kg b.w./day 수준으로 10주간 경구투여 하였을 때 염증 촉진 분자를 억제, 항염증 분자를 촉진함으로써 장 점액세포의 조직학적 및 기능적 회복을 유도하여 궁극적으로 대장염을 개선하였다. 이러한 결과를 근거로 PBL의 트립신 가수분해물이 고지방식이로 유도된 간 조직의 염증 반응을 개선할 수 있는 가능성을 제안할 수 있다.
한편, 본 연구에서 PBL 효소 가수분해물은 고지방식이로 인한 내당능의 손상을 개선시키는 경향을 나타냈다. 염증이 인슐린 저항성, 당 대사 이상과 밀접하게 연결되어 있으며, 염증 신호 경로의 억제가 당 대사 개선에 기여한다는 근거는 여러 연구에서 확인된 바 있다(Ullah et al. 2021). β-aminoisobutyric acid는 고지방식이 비만 유도 내당능 손상을 개선하였고, IκBα 인산화, NF-κB 핵 이동, 염증성 사이토카인을 유의하게 억제하였다(Jung et al. 2015). Jang et al.(2017)의 연구에서도, 짚신나물 물 추출물은 고지방식이를 공급한 랫드에서 내당능 반응 곡선의 30분, 60분, 120분 혈당을 유의하게 감소시켰고, 혈중 염증성 사이토카인(TNF-α, IL-6)을 감소시킨 반면 아디포넥틴은 증가시켰으며 이러한 효과는 간과 지방 조직 내 염증 관련 유전자의 발현 수준 감소를 수반하였다. 따라서 본 연구에서 관찰된 PBL 효소 가수분해물의 내당능 개선 경향은 염증 반응 억제와 연관된 기전에 의해 매개되었을 가능성을 시사한다.
본 연구의 제한점으로는 PBL 효소 가수분해물 투여가 일부 대사 지표 및 염증 관련 지표를 개선하는 경향을 보였으나, 내당능 및 간 조직의 염증 반응을 통계적으로 유의하게 개선시키지 못한 것이다. 본 연구에서는 단일 조건의 단백질 가수분해 효소를 사용하였으나, 효소의 종류에 따라 생성되는 펩타이드의 조성과 생리활성이 달라질 수 있다. 따라서 향후 연구에서는 가수분해 효소의 종류를 달리하거나, 효소 가수분해물의 투여 농도 및 기간을 다르게 하여 PBL 효소 가수분해물의 내당능 개선 및 항염증 효과를 탐색하기 위한 추가 연구가 필요할 것으로 사료 된다.
Ⅴ. 요약 및 결론
PBL은 단백질, 미량영양소, 불포화지방산 등을 함유하고 있는 우수한 단백질 급원으로, 약용 및 식용으로 사용되어 왔다. 생리활성 펩타이드는 체내에서 쉽게 흡수될 뿐만 아니라, 여러 생체 내 효소에 대한 저항성이 강해 기능성 펩타이드로서의 가치와 활용 가능성이 높으나, PBL에서 유래한 생리활성 펩타이드에 대한 연구는 미흡한 실정이다. 따라서, 본 연구에서는 고지방식이를 섭취한 마우스에서 PBL 효소 가수분해물이 당대사 및 지질대사에 미치는 영향을 알아보고자 하였다. 실험식이 공급 7주 후에, HD군에서 ND군에 비해 식이섭취량은 유의하게 감소하고, LDL-콜레스테롤과 TG 농도는 유의하게 증가하였으나, PBL 효소 가수분해물의 보충은 유의한 영향을 미치지 못하였다. OGTT 결과, 포도당 용액 섭취 후 30분의 혈당은 HD군에서 ND군에 비해 유의하게 증가하였으나, HDP군에서는 감소하는 경향을 보였다. 또한, 간 조직의 염증 관련 유전자인 TNF-α의 mRNA 발현 수준은 HD군에서 ND군에 비해 유의하게 증가하였으나, HDP군에서는 HD군에 비해 감소하는 경향이 있는 것으로 나타났다. 결론적으로, 고지방식이를 섭취한 마우스에서 PBL 효소 가수분해물은 OGTT에서 초기 30분 동안의 혈당 상승을 억제하고, TNF-α 유전자 발현 수준을 낮추는 경향을 보여주었다. 고지방식이를 섭취한 마우스에서 대사적 개선에 대한 PBL 효소 가수분해물의 농도별 및 장기적 효과를 검증하기 위한 추가적인 연구가 필요하다.
References
-
Ahn EM, Myung NY, Jung HA, Kim SJ(2019) The ameliorative effect of Protaetia brevitarsis Larvae in HFD-induced obese mice. Food Sci Biotechnol 28(4), 1177-1186.
[https://doi.org/10.1007/s10068-018-00553-w]

-
Blaisdell AP, Lau YL, Telminova E, Lim HC, Fan B, Fast CD, Garlick D, Pendergrass DC(2014) Food quality and motivation: a refined low-fat diet induces obesity and impairs performance on a progressive ratio schedule of instrumental lever pressing in rats. Physiol Behav 128, 220-225.
[https://doi.org/10.1016/j.physbeh.2014.02.025]

-
Francque SMA, Dirinck E(2023) NAFLD prevalence and severity in overweight and obese populations. Lancet Gastroenterol Hepatol 8(1), 2-3.
[https://doi.org/10.1016/S2468-1253(22)00375-2]

-
Hwang D, Goo T-W, Yun E-Y(2020) In vitro protective effect of paste and sauce extract made with Protaetia brevitarsis larvae on HepG2 cells damaged by ethanol. Insects 11(8), 494.
[https://doi.org/10.3390/insects11080494]

-
Im AR, Yang WK, Park YC, Kim SH, Chae S(2018) Hepatoprotective effects of insect extracts in an animal model of nonalcoholic fatty liver disease. Nutr 10(6),735.
[https://doi.org/10.3390/nu10060735]

-
Jang HH, Park MY, Kim HW, Lee YM, Hwang KA, Park JH, Park DS, Kwon O(2012) Black rice (Oryza sativa L.) extract attenuates hepatic steatosis in C57BL/6 J mice fed a high-fat diet via fatty acid oxidation. Nutr Metab 9(1), 27.
[https://doi.org/10.1186/1743-7075-9-27]

-
Jang HY, Kim JM, Kim JS, Kim BS, Lee YR, Bae JS(2023) Protaetia brevitarsis Extract Attenuates RANKL-Induced Osteoclastogenesis by Inhibiting the JNK/NF-κB/PLCγ2 Signaling Pathway. Nutr 15(14), 3193.
[https://doi.org/10.3390/nu15143193]

-
Jeong S, Jung J, Yang YS, Kim W, Cho IY, Lee Y, Park K, Nam GE, Han K, Taskforce Team of the Obesity Fact Sheet of the Korean Society for the Study of Obesity(2024) Obesity fact sheet: prevalence of obesity and abdominal obesity in adults, adolescents, and children in Korea from 2012 to 2021. J Obes Metab Syndr 33(1), 27-35.
[https://doi.org/10.7570/jomes24012]

-
Jung TW, Hwang HJ, Hong HC, Yoo HJ, Baik SH, Choi KM(2015) BAIBA attenuates insulin resistance and inflammation induced by palmitate or a high fat diet via an AMPK-PPARδ-dependent pathway in mice. Diabetologia 58(9), 2096-2105.
[https://doi.org/10.1007/s00125-015-3663-z]

-
Kwon HJ, Chun SY, Lee EH, Yoon B, Han MH, Chung JW, Ha YS, Lee JN, Kim HT, Kim DH, Kwon TG, Kim BS, Lee SO, Jang BI(2023) Protaetia brevitarsis-derived protein hydrolysate reduces obesity-related colitis induced by high-fat diet in mice through anti-inflammatory pathways. Int J Mol Sci 24(15), 12333.
[https://doi.org/10.3390/ijms241512333]

-
Larsson SC, Burgess S(2021) Causal role of high body mass index in multiple chronic diseases: a systematic review and meta-analysis of Mendelian randomization studies. BMC Med 19(1), 320.
[https://doi.org/10.1186/s12916-021-02188-x]

-
Lee EH, Chun SY, Yoon B, Han MH, Chung JW, Ha YS, Lee JN, Kim HT, Kim DH, Beik GY, Jang BI, Kwon TG, Park CE, Lee IS, Kim BS, Lee SO(2022) Antiobesity and Hepatoprotective Effects of Protein Hydrolysates Derived from Protaetia brevitarsis in an Obese Mouse Model. Biomed Res Int 2022, 4492132.
[https://doi.org/10.1155/2022/4492132]

-
Lee HS, Ryu HJ, Song HJ, Lee SO(2017) Enzymatic preparation and antioxidant activities of protein hydrolysates from Protaetia brevitarsis larvae. J Korean Soc Food Sci Nutr 46(10), 1164-1170.
[https://doi.org/10.3746/jkfn.2017.46.10.1164]

- Ministry of Agriculture, Food and Rural Affairs(2025) 2024 Survey on the Actual Condition of the Insect Industry
-
Nasri M(2017) Protein hydrolysates and biopeptides: production, biological activities, and applications in foods and health benefits. A Review. Adv Food Nutr Res 81, 109-159.
[https://doi.org/10.1016/bs.afnr.2016.10.003]

-
Okunogbe A, Nugent R, Spencer G, Powis J, Ralston J, Wilding J(2022) Economic impacts of overweight and obesity: current and future estimates for 161 countries. BMJ Glob Health 7(9), e009773.
[https://doi.org/10.1136/bmjgh-2022-009773]

-
Park CE, Lee SO(2023) Nrf2-mediated protective effect of protein hydrolysates from Protaetia brevitarsis larvae against oxidative stress-induced hepatotoxicity. Food Sci Biotechnol 32(11), 1561-1571.
[https://doi.org/10.1007/s10068-023-01279-0]

- Park S, Yun E(2018) Edible insect food: current scenario and future perspectives. Food Sci Anim Resour 7(1), 12-20
-
Park WJ, Oh E, Kim Y(2024) Protaetia brevitarsis larvae extract protects against lipopolysaccharides-induced ferroptosis and inflammation by inhibiting acid sphingomyelinase. Nutr Res Pract 18(5), 602-616.
[https://doi.org/10.4162/nrp.2024.18.5.602]

-
Park YM, Noh EM, Lee HY, Shin DY, Lee YH, Kang YG, Na EJ, Kim JH, Yang HJ, Kim MJ, Kim KS, Bae JS, Lee YR(2021) Anti-diabetic effects of Protaetia brevitarsis in pancreatic islets and a murine diabetic model. Eur Rev Med Pharmacol Sci 25(23), 7508-7515.
[https://doi.org/10.26355/eurrev_202112_27450]

-
Petrie JR, Guzik TJ, Touyz RM(2018) Diabetes, hypertension, and cardiovascular disease: clinical insights and vascular mechanisms. Can J Cardiol 34(5), 575-584.
[https://doi.org/10.1016/j.cjca.2017.12.005]

-
Tang C, Wang Y, Xu Z, Chen D, Xu J, Yang D, Zhang L, Liu J, Kan J(2024) The relationships between high-fat diet and metabolic syndrome: potential mechanisms. Food Bioscience 59, 104261
[https://doi.org/10.1016/j.fbio.2024.104261]

-
Tyrrell J, Mulugeta A, Wood AR, Zhou A, Beaumont RN, Tuke MA, Jones SE, Ruth KS, Yaghootkar H, Sharp S, Thompson WD, Ji Y, Harrison J, Freathy RM, Murray A, Weedon MN, Lewis C, Frayling TM, Hyppönen E(2019) Using genetics to understand the causal influence of higher BMI on depression. Int J Epidemiol 48(3), 834-848.
[https://doi.org/10.1093/ije/dyy223]

-
Ullah R, Rauf N, Nabi G, Yi S, Yu-Dong Z, Fu J(2021) Mechanistic insight into high-fat diet-induced metabolic inflammation in the arcuate nucleus of the hypothalamus. Biomed Pharmacother 142, 112012.
[https://doi.org/10.1016/j.biopha.2021.112012]

- Winichagoon P, Margetts BM(2017) The double burden of malnutrition in low- and middle-income countries. In: Romieu I, Dossus L, Willett WC, editors. Energy Balance and Obesity. Lyon (FR): International Agency for Research on Cancer(IARC Working Group Reports, No. 10.) CHAPTER 2. Available from https://www.ncbi.nlm.nih.gov/books/NBK565820/, [cited 2026 January 2]