익모초 추출물의 항산화 효과 및 MCF-7 유방암 세포주의 성장억제 유도에 관한 연구
This is an Open-Access article distributed under the terms of the Creative Commons Attribution Non-Commercial License (http://creativecommons.org/licenses/by-nc/3.0), which permits unrestricted non-commercial use, distribution, and reproduction in any medium, provided the original work is properly cited.
Abstract
Many studies have shown that phytochemicals in plants are effective in preventing and treating many cancers. Leonurus sibiricus L. (LS) is a plant widely used for the treatment of inflammatory conditions. However, the role of the anticancer effects of LS extract concerning breast cancers has not been examined. Our study investigated the antioxidant and anticancer effect of LS extract using MCF-7 cells (human breast cancer cell line). LS extract contained high total polyphenol (198.30 mg TAE/g) and total flavonoid (118.91 mg RE/g) contents as well as effective ABTS+ free radical scavenging capacity. LS extract at 0.1, 0.2, 0.4, and 0.8 mg/mL concentrations significantly inhibited the MCF-7 cells proliferation for 24 h and 48 h. Apoptotic bodies were observed in DAPI stained treated cells with LS extract under a fluorescence microscope. Furthermore, LS extract treatment showed increasing cleaved PARP protein expression while decreasing Bcl-2 and phospho-Akt levels. These results suggest that LS extract could be a promising chemopreventive agent for breast cancers.
Keywords:
Leonurus sibiricus L, antioxidant activity, cell growth, apoptosis, breast cancerI. 서론
유방암은 우리나라를 포함한 전 세계 여성들에게 높은 발병률 및 사망률을 보이고 있으며, 이를 통한 위험 비중이 높아지고 있다(Ghoncheh et al. 2016). 유방암의 일반적인 치료법으로는 수술, 화학요법, 방사선요법 및 항암제 이용 등이 있으나, 일부는 정상세포의 파괴와 항암제의 내성 획득으로 인해 인체에 심각한 부작용을 일으킨다고 보고되었다(Hernandez-Aya et al. 2013). 따라서 임상치료의 성공을 위해 유방암에 대한 효과적인 치료법의 모색이 더욱 필요하다고 할 수 있겠다.
암을 일으키는 여러 발생원인 중, 생체 내에서 필요한 에너지 공급을 위해 끊임없이 발생하는 활성산소(reactive oxygen species, ROS)와 여러 환경적 요인에 의해 발생하는 산화적 스트레스가 주목받고 있으며, 이들을 제어하기 위한 항산화 시스템에 대한 연구가 활발히 진행 중이다(Dragsted et al. 1993). 또한 암세포의 제한 없는 증식과 자가세포사멸(apoptosis)의 억제를 제어하는 것이 효과적인 암 치료 방법 중 하나로 여겨진다. 지금까지 여러 역학조사에 의해 식용식물에 포함된 여러 가지 생리활성물질들이 암을 포함한 만성질환의 예방 및 치료에 효과적이라 밝혀졌으며(Lee et al. 2011), 이들은 여러 산화적 손상으로부터 신체를 보호하며 세포의 성장에 관여하는 신호전달체계를 조절함으로서 암의 발생 및 위험을 줄일 수 있다고 보고되었다(Dragsted et al. 1993).
익모초는 꿀풀과에 속하는 두해살이풀로 네모난 줄기에 잎과 꽃으로 되어 있으며 한국, 중국, 일본 등을 포함한 아시아와 유럽에서 자생하는 것으로 알려져 있다(Wu et al. 2011). 익모초의 약효로는 산후의 출혈, 월경불순, 무월경, 고혈압, 감기, 기관지염 등 이며, 그 중 잎은 구토와 설사, 류머티즘, 피부염을 치료하는데 효과가 있다고 보고되었다(Castellucci et al. 2000; Almeida et al. 2011). 또한 항균, 항염증, 항통각 및 항산화 작용 등과 같은 생물학적 활성을 가지고 있는 것으로 알려졌다(Islam et al. 2005; Ahmed et al. 2006; Shin et al. 2009; Lee et al. 2017; Oliveira et al. 2017). 익모초에 함유된 주요 성분으로는 phenol(chlorogenic acid, ferulic acid, caffeic acid)과 flavonoid(wogonin, quercetin, hyperoside) 및 alkaloid(leonurine, stachydrine) 등이다(Shang et al. 2014; Oliveira et al. 2017). 식물 내 주요성분들은 오랜 역사를 통한 항암제의 원천으로 큰 기여를 하고 있으며, 실제 항암효과를 나타내는 약물의 약 25% 이상이 천연물 유래로 만들어졌다(Farnsworth 1990). 이러한 이유로 천연물이 가지고 있는 항산화 효능 및 항암 등의 다양한 생리활성 기능을 밝히는 것은 매우 중요하다고 할 수 있겠다. 따라서 본 연구에서는 익모초 추출물을 이용한 항산화 활성 측정 및 인간유래 유방암 세포주인 MCF-7 세포주를 이용하여 apoptosis 유도에 의한 항암작용에 대해 연구하고자 한다.
Ⅱ. 연구방법
1. 재료
본 실험에 사용된 익모초는 ㈜우진티유플랜에서 분말형태로 2017년 12월에 구입하였다. 100 g의 익모초 분말과 80% 에탄올 1.5 L을 첨가하여 환류냉각관이 부착된 65℃ heating mantle(Mtops ms-265, Seoul, Korea)을 이용하여 3시간씩 3회 추출하고 Whatman filter paper(Whatman No. 2)로 여과시켰다. 여액을 rotary vacuum evaporator(VACUUM NVC-1100, EYELA Co., Ltd., Tokyo, Japan)를 이용하여 감압 농축하고 동결건조하여 –70℃ deep freezer(MDFU52V, Sanyo Electric Co., Ltd., Osaka, Japan)에 보관하여 사용하였다.
2. Total flavonoid 및 Total polyphenol 함량 측정
Total flavonoid 함량은 Davis법을 일부 변형한 Chae 등의 방법(2002)에 따라 측정하였다. Diethylene glycol(Sigma, St, Louis, MO, USA)에 1 mg/mL 농도의 익모초 에탄올 추출물 0.5 mL를 첨가하고 충분히 섞어주었다. 1N NaOH를 10 µL를 넣고 37℃에서 1시간 반응시킨 후 UV-spectrophotometer(Bio-Rad, Hercules, CA, USA)로 420 nm에서 흡광도를 측정하였다. Rutin(Sigma, St, Louis, MO, USA)을 표준물질로 이용하여 표준검량곡선을 적용해 익모초 추출물의 total flavonoid 함량을 계산하였다.
Total polyphenol 함량은 Folin-Denis의 방법(1912)에 따라 측정하였다. 익모초 에탄올 추출물 0.5 mL에 Folin reagent(Sigma-Aldrich Inc., St. Louis, MO, USA) 0.5 mL를 첨가한 후 3분 동안 실온에서 반응시킨다. 10% Na2CO3용액 0.4 mL를 첨가하고 암소에서 40분 동안 반응시킨 후에 UV-spectrophotometer(Bio-Rad Laboratories, Inc., Hercules, CA, USA)를 이용하여 760 nm에서 흡광도를 측정하였다. Tannic acid(Sigma, St. Louis, MO, USA)를 표준물질로 하여 표준검량곡선을 적용해 익모초 추출물의 total polyphenol 함량을 계산하였다.
3. ABTS+ radical 소거능 측정
익모초 추출물의 ABTS+ 라디칼 소거능은 Re의 방법(1999)을 변형하여 측정하였다. 7 mM 2,2-azinobis-3-ethylbenzothiazoline-6-sulfonic acid(ABTS, Sigma, St. Louis, MO, USA )에 2.4 mM potassium persulfate를 1 : 1 비율로 혼합해 암소에서 24시간 반응시켰다. 반응이 끝난 ABTS 시약을 734 nm에서의 흡광도 값이 0.7~1.0로 되게 희석하여 사용하였다. 희석한 ABTS 용액 900 µL와 0.125, 0.25, 0.5, 1 mg/mL 농도의 시료 100 µL를 혼합하여 37℃에서 30분 동안 반응시킨 후, 96 well plate에 200 µL씩 분주하여 734 nm에서 흡광도에서 UV-spectrophotometer(Bio-Rad, Hercules, CA, USA)를 이용하여 측정하였다.
4. 세포배양
본 실험에 사용된 인체 유방암세포주인 MCF-7은 한국세포주은행(Korean Cell Line Bank, Seoul, Korea)으로부터 분양 받아 사용하였다. 10% fetal bovine serum(FBS)과 1% penicillin/streptomycin을 포함한 RPMI1640 배지(Gibco-BRL, Grand Island, NY, USA)를 사용하였으며, 37℃, 5% CO2 incubator (MCO-18AIC, Sanyo, Osaka, Japan)에서 계대 배양하여 사용하였다.
5. MTS assay
세포배양용 96 welll plate에 MCF-7 세포(2×103 cells/well)를 분주하고 24시간 배양한 후, dimethyl sulfoxide(DMSO)에 녹인 익모초 에탄올 추출물을 0.1, 0.2, 0.4, 0.8 mg/mL 농도로 세포에 처리하였다. 이를 24시간 또는 48시간 처리 후, 각 well에 CellTiter 96® AQueous One Solution Cell Proliferation Assay(MTS) 용액(Promega Co., CA, USA)을 20 µL 첨가하여 37℃, 5% CO2 incubator(MCO-18AIC, Sanyo, Osaka, Japan)에서 4시간 동안 반응시키고 UV-spectrophotometer(Bio-Rad, Hercules, CA, USA)를 이용하여 490 nm에서 흡광도를 측정하였다.
6. MCF-7 유방암세포 형태 관찰
MCF-7 세포의 형태를 관찰하기 위해 60 mm dish에 MCF-7 세포(4×105 cells/well)를 분주하였다. 24시간 배양한 후, 익모초 에탄올 추출물 0.2 mg/mL와 0.4 mg/mL를 48시간 동안 처리한 한 후에 광학현미경(CKX41, OLIMPUS Co., Tokyo, Japan)을 이용하여 MCF-7 세포의 형태 변화를 100배율로 관찰하였다.
7. DAPI staining
Apoptosis가 유발된 경우 특이적으로 핵에 나타나는 변화를 관찰하기 위하여 12 well plate에 MCF-7 세포(1×105 cells/well)를 분주하고 24시간 배양한 후에, 익모초 에탄올 추출물 0.2 mg/mL와 0.4 mg/mL를 각각 처리하여 37℃, 5% CO2 incubator(MCO-18AIC, Sanyo, Osaka, Japan)에서 배양하였다. 48시간 후에 배지를 제거하고 phosphate buffered saline (PBS)을 이용하여 세척하였으며 4% paraformaldehyde solution(Biosesang, Seongnam, Korea)에 1시간 고정하였다. 그 후, 상층액을 제거하고 0.5% Triton X-100 solution(Sigma, St. Louis, MO, USA)을 10분간 처리하였으며 4,6-diamidino-2-phenylindole(DAPI) staining 용액(Vector laboratories, Burlingame, CA, USA)으로 염색한 후에 콘포칼 현미경(LSM 520, Zeiss, oberkochen, Germany)을 이용하여 100배율로 apoptosis 형태를 관찰하였다.
8. Western Blotting
60 mm dish에 MCF-7 세포(4×105 cells/well)를 24시간 배양한 다음, 익모초 에탄올 추출물을 0.2 mg/mL와 0.4 mg/mL를 각각 처리하여 37℃, 5% CO2 incubator(MCO-18AIC, Sanyo, Osaka, Japan)에서 48시간 배양하였다. 배양이 끝난 세포에 cell lysis buffer(150 mM NaCl, 0.1% SDS, 1% Triton X-100, 50 mM Tris-Hcl, pH 8.0)를 첨가한 후, 14,000 rpm에서 원심분리 하여 상등액을 분리하였다. Bradford assay(Bio-Rad, CA, USA)를 사용하여 단백질을 정량한 후에 10% sodium dodecyl sulfate-polyacrylamide gel electrophoresis(SDS-PAGE)로 전기영동하고 이를 polyvinylidene difluoride(PVDF) membranes (Bedford, MA, USA)에 옮겨 transfer한 후, 5% skim milk를 이용해 1시간 동안 blocking하였다. 각각의 1차 antibody를 4℃에서 overnight하고, 2차 antibody를 상온에서 1시간 반응시킨 후에 암실에서 enhanced chemiluminoesence solution(Amersham Biosciences Co., Buckinghamshire, UK)을 이용하여 X-ray film에 감광시켜 단백질의 발현을 확인하였다. 실험에 사용된 1차 antibody인 Akt, phospho-Akt, poly(ADP-ribose) polymerase(PARP), Bcl-2, β-actin과 2차 antibody인 horseradish peroxidase (HRP)-conjugated anti-mouse는 Santa Cruz(Santa Cruz Biotechnology Inc., CA, USA)에서 구입하여 사용하였다.
9. 통계처리
실험의 측정 결과는 평균(mean)과 표준편차(SD)로 나타내었으며 모든 실험은 독립적으로 3회 반복을 통해 얻었다. 각 실험군 간의 유의성 검증은 GraphPad Prism 6 program(GraphPad Software, Inc., La Jolla, CA, USA)을 이용하였고, 각 시료간의 통계적 유의성은 p<0.05 수준에서 Student t-test를 이용하여 유의성을 검정하였다.
Ⅲ. 결과 및 고찰
1. 익모초 에탄올 추출물의 추출수율 및 항산화 성분 함량
익모초 에탄올 추출물의 추출수율과 total flavonoid 및 total polyphenol 함량을 분석하여 Table 1에 나타내었다. 추출수율이 낮으면 추출물의 생리활성 효과가 뛰어나더라도 기능성식품 원료로서의 활용이 어려우며(Kim et al. 2017), 10% 이상의 추출수율을 얻어야 경제적 활용 가능성이 있다고 판단되어진다(Park et al. 2011). 본 실험의 익모초 추출수율은 34.50%로 나타났으며, 이를 통해 익모초 추출물은 기능성식품 원료로서의 활용 가능성이 높은 소재라 여겨진다. 천연물이 함유하고 있는 flavonoid 및 polyphenol 화합물은 생체 내에서 항산화, 항암, 항비만 등의 생리활성을 나타내는 것으로 알려져 있으며, 이러한 효과를 보이는 생리활성 물질들을 추출하여 활용하려는 연구가 활발히 이루어지고 있다(Hwang et al. 2013). 본 연구에 사용된 익모초 에탄올 추출물의 total flavonoid 함량은 118.91 mg RE/g, total polyphenol 함량은 198.30 mg TAE/g으로 나타났다. 꿀풀과에 속하는 속단(Kim et al. 2011)과 단삼 추출물(Yang et al. 2007)의 경우, total polyphenol 함량이 각각 57.32 mg TAE/g과 77.58 mg TAE/g으로 나타나 본 연구와의 차이를 보였다.
2. 익모초 에탄올 추출물의 ABTS+ radical 소거능 측정
항산화 작용은 생체 내에 존재하는 활성 radical을 안정한 형태의 radical로 전환시켜 산화를 억제시키는 것으로, 이러한 radical 소거능이 뛰어난 경우 항산화 활성이 높다고 할 수 있다(Yun et al. 2015). 본 연구에 사용된 익모초 에탄올 추출물의 ABTS+ radical 소거능은 0.125, 0.25, 0.5, 1.0 mg/mL 농도에서 각각 19.20, 32.31, 56.89, 88.44%의 ABTS+ radical 소거능을 나타내었으며, 50%의 radical 소거능을 나타내는 값인 IC50은 0.43 mg/mL로 나타났다. 익모초의 ABTS+ radical 소거능을 측정한 선행 연구를 보면, IC50값이 1.0 mg/mL로 본 연구보다 높은 농도에서 동일한 효과를 보였다(Seo et al. 2013). 또한, Oliveira et al (2017)이 익모초 에탄올 추출물을 이용한 ABTS+ radical 소거능을 측정한 결과, 2.5 mg/mL과 5 mg/mL에서 유의적으로 감소하였다고 하며, 본 연구와 다소 차이를 보였다.
3. 익모초 에탄올 추출물이 MCF-7 세포의 성장에 미치는 영향
익모초 에탄올 추출물이 인체 유방암세포주인 MCF-7 세포의 증식에 미치는 영향을 조사하기 위하여 익모초 에탄올 추출물을 0.1, 0.2, 0.4, 0.8 mg/mL 농도별로 처리한 후, MTS assay를 통해 확인하였다. Fig. 1A에서 나타난 것과 같이 MCF-7 세포에 익모초 에탄올 추출물을 24시간 처리하였을 경우, 0.4 mg/mL과 0.8 mg/mL 농도에서 각각 36%와 55%의 유의적 세포증식 억제효과를 보였고, 48시간 처리하였을 때 0.2, 0.4, 0.8 mg/mL 농도에서 대조군에 비해 23, 57, 83%의 유의적 세포증식 억제효과를 나타내었다. 이는 동일한 농도의 익모초 에탄올 추출물에서 처리시간이 길어짐에 따라 암세포주의 증식이 억제됨을 확인하였다. Kim et al (2018)은 인체 유방암 세포인 MCF-7에 꿀풀과에 속하는 곰보배추 에탄올 추출물을 48시간 동안 처리하였을 때, 0.2 mg/mL 처리농도에서부터 농도 의존적인 암세포 증식 억제효과를 나타내었으며 본 연구와 유사함을 보였다. 또한 익모초 에탄올 추출물 처리에 따른 암세포의 형태 변화를 관찰한 결과는 Fig. 1B와 같다. MCF-7 세포에 0.2 mg/mL과 0.4 mg/mL의 익모초 에탄올 추출물을 48시간 처리하였을 경우, 대조군과 비교하여 부착되어 있는 세포가 적고 세포의 변형이 관찰되었으며 배지에 떠있는 세포가 증가하였다. 이와 같은 결과는 익모초 에탄올 추출물이 인체 유방암 세포인 MCF-7의 부착과 증식을 억제하고 세포를 손상시켜 세포사멸을 촉진하는 것으로 판단된다.
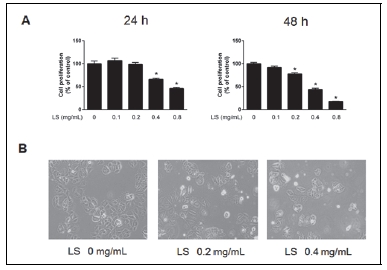
Growth inhibitory effect of LS extract on MCF-7 breast cancer cells. (A) Cells were treated with LS extract (0.1, 0.2, 0.4 and 0.8 mg/mL) for 24 h and 48 h by MTS assay. (B) Morphological changes were visualized by light microscopy after LS extract treatment for 48 h (magnification × 100). All the values are expressed as the mean ± SD of at least three replicate experiments. Significantly different (p<0.05) compared with the DMSO-control.
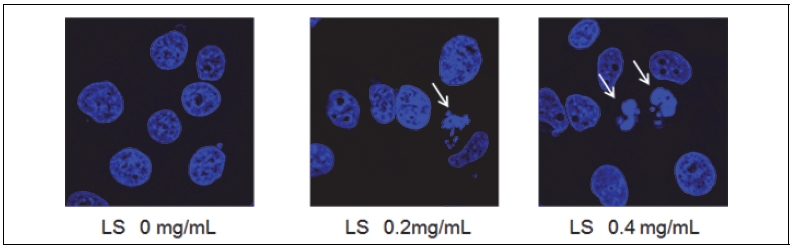
4. 익모초 에탄올 추출물이 DAPI staining을 통한 apoptosis 관찰
정상세포는 세포의 변이가 일어났을 경우 스스로 죽음을 선택해 변이세포를 생성하지 못하도록 apoptosis 시스템을 구축하고 있다. 하지만 암세포의 경우, 변이가 일어나도 apoptosis가 정상적으로 일어나지 않고 세포가 증식하는 특징이 있다. 세포가 apoptosis를 일으키면 세포질과 염색체의 형태학적 변화를 일으켜 apoptotic body가 형성된다. 이를 확인하기 위해 본 연구에서는 MCF-7 세포에 익모초 에탄올 추출물 처리 후, DAPI 염색을 실시하고 형광현미경을 이용하여 관찰하였다. Fig. 2에 나타난 바와 같이 익모초 에탄올 추출물을 각각 0.2 mg/mL와 0.4 mg/mL 농도로 48시간 처리하였을 때, 정상세포에 비해 익모초 처리한 군에서 염색질이 응축된 apoptotic body가 농도 의존적으로 증가함을 확인하였다. 이와 같은 결과로 볼 때, 익모초 에탄올 추출물에 의한 MCF-7 세포의 증식 억제와 형태 변화는 apoptosis와 연관성이 있음을 알 수 있었다.
5. 익모초 에탄올 추출물이 PARP와 Bcl-2 단백질 발현에 미치는 영향
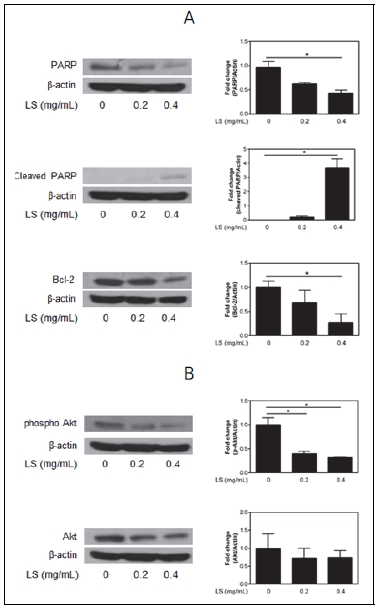
Poly(ADP ribose) polymerase(PARP)는 손상된 DNA를 복구하는 단백질로 핵 안에 존재하며 caspase에 의해 분절되어 apoptosis를 유도한다(Yoon et al. 2012). 정상세포의 PARP는 분자량이 116 kDa지만 apoptosis가 유도된 세포의 PARP는 85 kDa에 분절된 형태가 관찰된다(Lee et al. 2016). Bcl-2 family는 anti-apoptotic 단백질(Bcl-2, Bcl-xL)과 pro-apoptotic 단백질(Bax, Bak, Bid)로 구분되며, 미토콘드리아의 막에 존재하거나 apoptosis 유도에 의해 미토콘드리아의 내적 경로에 의해 apoptosis를 조절한다. Pro-apoptotic 단백질인 Bax가 세포질에서 미토콘드리아로 이동하면 cytochorome C가 방출되어 apoptosis가 유도되고, anti-apoptotic 단백질인 Bcl-2는 Bax의 이동을 억제하여 apoptosis의 유도를 억제한다(Lee et al. 2016). 본 연구에서는 익모초 에탄올 추출물이 MCF-7 세포의 apoptosis 유도에 관여하는지 알아보고자 하였다. 그 결과, 익모초 에탄올 추출물을 각각 0.2 mg/mL과 0.4 mg/mL 농도로 처리하였을 경우, caspase-3 기질의 하나인 PARP의 발현은 유의적으로 감소하였고 cleaved-PARP의 단백질 발현은 농도 의존적으로 증가하였음을 관찰하였으며, Bcl-2의 단백질 발현은 유의적으로 감소하였다(Fig. 3A). 암세포에서 Bcl-2의 과발현은 항암제의 내성에 관련되어 있다고 알려져 있으며(Debatin 2004), 익모초 추출물에 의한 Bcl-2의 단백질 발현을 감소는 apoptosis 유도와 연관이 있다고 사료된다.
6. 익모초 에탄올 추출물이 PI3K/Akt 단백질 발현에 미치는 영향
Phosphatidylionositol 3-kinase(PI3K)/Akt 경로는 apoptosis를 저해하고 세포의 생존을 증가시키는 역할을 하며(Kim et al. 2016), 여러 암종에서 Akt의 발현은 비정상적으로 높다고 알려져 있다(Park et al. 2011). 본 연구에서는 익모초 에탄올 추출물이 MCF-7 세포의 PI3K/Akt 경로에 미치는 영향에 대해 알아보고자 하였다. Fig. 3B에 나타난 바와 같이 익모초 에탄올 추출물에 의해 Akt의 발현은 유의적인 차이가 없었으나 활성형태인 phospho Akt의 발현이 익모초 에탄올을 처리한 군에서 유의적으로 감소함을 나타내었다.
Ⅳ. 요약 및 결론
본 연구는 익모초 에탄올 추출물의 total polyphenol 및 total flavonoid 함량, ABTS+ assay를 이용한 free radical 소거능을 측정하였으며, 인체 유래 유방암세포인 MCF-7 세포를 사용하여 익모초 에탄올 추출물에 의한 유방암 세포의 증식 억제 효과에 관하여 조사하였다. 익모초 에탄올 추출물의 total polyphenol 함량은 198.30 mg TAE/g, total flavonoid 함량은 118.91 mg RE/g로 측정되었으며, ABTS+ assay를 이용한 IC50은 0.43 mg/mL으로 나타났다. MCF-7 유방암 세포주에 익모초 에탄올 추출물 0.1, 0.2, 0.4, 0.8 mg/mL을 24시간과 48시간 처리한 경우, 유방암세포의 증식이 유의적으로 억제됨을 확인하였다. 또한, DAPI staining을 통해 apoptosis에 의한 세포질의 응축과 핵이 분절되는 apoptotic body가 농도 의존적으로 증가됨을 관찰하였다. 익모초 에탄올 추출물에 의해 변화하는 apoptosis 관련 단백질의 발현을 관찰하기 위해 western blotting을 수행한 결과, PARP의 발현이 감소하며 cleaved PARP의 발현은 증가함을 보였다. 반면, anti-apoptotic 단백질인 Bcl-2와 phospho Akt의 단백질 발현이 억제됨을 확인하였다. 이상의 결과를 통하여 익모초 에탄올 추출물은 높은 항산화활성을 가지고 있으며, 유방암세포에서 apoptosis 유도에 의한 항암효과를 가지고 있는 것으로 판단되며, 향후 암의 예방 및 치료를 위한 기초자료로 사용될 수 있을 것으로 사료된다.
Acknowledgments
This research was supported by grants from National Research Foundation of Korea(NRF-2017R1C1B1007646)
References
-
Ahmed, F, Islam, MA, Rahman, MM, (2006), Antibacterial activity of Leonurus sibiricus aerial parts, Fitoterapia, 77(4), p316-317.
[https://doi.org/10.1016/j.fitote.2006.03.005]

- Almeida, LFR, Polleto, RS, Pinho, SZ, Delachiave, MEA, (2011), Methodology for Leonurus sibiricus L. seed germination, Braz J Med Plants, 13(2), p190-196.
- Castellucci, S., Lima, MIS, Nordi, N, Marques, JGW, (2000), Medicinal plants used by the local inhabitants of the Jatai ecological station, Luiz Antonio, Sao Paulo, Brazil: an ethnobotanical study, Braz J Med Plants, 3, p51-60.
- Chae, SK, Kang, GS, Ma, SJ, Bang, KW, Oh, MW, Oh, SH, (2002), Standard food analysis, Paju, Jigu-Moonwha Sa, p381-382.
-
Debatin, KM, (2004), Apoptosis pathways in cancer and cancer therapy, Cancer Immunol Immunother, 53(3), p153-159.
[https://doi.org/10.1007/s00262-003-0474-8]

-
Dragsted, LO, Strube, M, Larsen, JC, (1993), Cancer-protective factors in fruits and vegetables: biochemical and biological background, Pharmacol Toxicol, 72(1), p116-135.
[https://doi.org/10.1111/j.1600-0773.1993.tb01679.x]

-
Farnsworth, NR, (1990), The role of ethnopharmacology in drug development, Ciba Found Symp, 154, p2-11.
[https://doi.org/10.1002/9780470514009.ch2]

- Folin, O, Denis, W, (1912), On phosphotungstic-phosphomolybdic compounds as color reagents, J Biol Chem, 12(2), p239-249.
-
Ghoncheh, M, Pournamdar, Z, Salehiniya, H, (2016), Incidence and mortality and epidemiology of breast cancer in the world, Asian Pac J Cancer Prev, 17(S3), p43-46.
[https://doi.org/10.7314/APJCP.2016.17.S3.43]

-
Hernandez-Aya, LF, Gonzalez-Angulo, AM, (2013), Adjuvant systemic therapies in breast cancer, Surg Clin North Am, 93(2), p473-491.
[https://doi.org/10.1016/j.suc.2012.12.002]

-
Hwang, SY, Choi, HM, Lim, SY, (2013), Total phenolics of dried platycodon grandiflorum and its effect on growth of human cancer cell lines, Korean J Food Sci Technol, 45(1), p84-89.
[https://doi.org/10.9721/kjfst.2013.45.1.84]

-
Islam, MA, Ahmed, F, Das, AK, Bachar, SC, (2005), Analgesic and anti-inflammatory activity of Leonurus sibiricus, Fitoterapia, 76(3-4), p359-362.
[https://doi.org/10.1016/j.fitote.2005.03.014]

-
Kim, EJ, Kim, GT, Kim, BM, Lim, EG, Ha, SH, Kim, SY, Kim, YM, (2016), Apoptotic effect of extract from Artemisia annua Linné by Akt/mTOR/GSK-3β signal pathwayin Hep3B human hepatoma cells, J Life Sci, 26(7), p764-771.
[https://doi.org/10.5352/jls.2016.26.7.764]

-
Kim, HA, Lee, JM, (2018), Effect of antioxidant activities and apoptosis induction of Salvia plebeia R. Br. in human breast cancer MCF-7 cells, Korean J Community Living Sci, 29(2), p197-205.
[https://doi.org/10.7856/kjcls.2018.29.2.197]

-
Kim, HJ, Kim, MJ, Oh, SI, Jung, YT, Park, SK, Lee, IS, (2011), Quality characteristics and storage improvement of seasoned pork added with Phlomis umbrosa Turcz. extracts, J Korean Soc Food Sci Nutr, 40(1), p102-109.
[https://doi.org/10.3746/jkfn.2011.40.1.102]

-
Kim, YK, Son, HK, Lee, JJ, (2017), Nutritional components and antioxidant activities of various stachys Sieboldii Miq Parts, Korean J Community Living Sci, 28(2), p203-215.
[https://doi.org/10.7856/kjcls.2017.28.2.203]

-
Lee, HN, Shin, SA, Choo, GS, Kim, HJ, Park, YS, Kim, SK, Jung, JY, (2016), Inhibitory effects of spinach, cabbage, and onion extracts on growth of cancer cells, J Korean Soc Food Sci Nutr, 45(5), p671-679.
[https://doi.org/10.3746/jkfn.2016.45.5.671]

-
Lee, KW, Bode, AM, Dong, Z, (2011), Molecular targets of phytochemicals for cancer prevention, Nat Rev Cancer, 11(3), p211-218.
[https://doi.org/10.1038/nrc3017]

- Lee, MJ, Lee, HS, Park, SD, Moon, HI, Park, WH, (2017), Leonurus sibiricus herb extract suppresses oxidative stress and ameliorates hypercholesterolemia in C57BL/6 mice and TNF-alpha induced expression of adhesion molecules and lectin-like oxidized LDL receptor-1 in human umbilical vein endothelial cells, Biosci Biotechnol Biochem, 74(2), p279-284.
-
Oliveira, AS, Cercato, LM, de Santana Souza, MT, Melo, AJO, Lima, BDS, Duarte, MC, Araujo, AAS, de Oliveira, E, Silva, AM, Camargo, EA, (2017), The ethanol extract of Leonurus sibiricus L. induces antioxidant, antinociceptive and topical anti-inflammatory effects, J Ethnopharmacol, 206, p144-151.
[https://doi.org/10.1016/j.jep.2017.05.029]

-
Park, SY, Lee, SH, Park, OJ, Kim, YM, (2011), Apoptotic effects of curcumin and EGCG via Akt-p53 signaling pathway in HCT116 colon cancer cells, J Life Sci, 21(1), p89-95.
[https://doi.org/10.5352/jls.2011.21.1.89]

-
Re, R, Pellegrini, N, Proteggente, A, Pannala, A, Yang, M, Rice-Evans, C, (1999), Antioxidant activity applying an improved ABTS radial cation decolorization assay, Free Radic Biol Med, 26(9-10), p1231-1237.
[https://doi.org/10.1016/s0891-5849(98)00315-3]

-
Shang, X, Pan, H, Wang, X, He, H, Li, M, (2014), Leonurus japonicus Houtt.: ethnopharmacology, phytochemistry and pharmacology of an important traditional Chinese medicine, J Ethnopharmacol, 152(1), p14-32.
[https://doi.org/10.1016/j.jep.2013.12.052]

-
Shin, HY, Kim, SH, Kang, SM, Chang, IJ, Kim, SY, Jeon, H, Leem, KH, Park, WH, Lim, JP, Shin, TY, (2009), Anti-inflammatory activity of Motherwort (Leonurus sibiricus L.), Immunopharmacol Immunotoxicol, 31(2), p209-213.
[https://doi.org/10.1080/08923970802135443]

-
Wu, H, Fronczek, FR, Ferreira, D, Burandt, CL Jr, Zjawiony, JK, (2011), Labdane diterpenoids from Leonurus sibiricus, J Nat Prod, 74(4), p831-836.
[https://doi.org/10.1021/np100956k]

- Yang, SA, Im, NK, Lee, IS, (2007), Effects of methanolic extract from Salvia miltiorrhiza Bunge on in vitro antithrombotic and antioxidative activities, Korean J Food Sci Technol, 39(1), p83-87.
-
Yoon, HJ, Lee, S, Hwang, IK, (2012), Effects of green pepper (Capsicum annuum var.) on antioxidant activity and induction of apoptosis in human breast cancer cell lines, Korean J Food Sci Technol, 44(6), p750.
[https://doi.org/10.9721/kjfst.2012.44.6.750]

-
Yun, SG, Jeong, HY, Yun, HJ, Do, MY, Kim, BW, Kwon, HJ, (2015), Anti-oxidant, anti-inflammatory and anti-cancer effect of methanol extract of Pogostemon cablin, J Life Sci, 25(1), p44-52.
[https://doi.org/10.5352/jls.2015.25.1.44]